פרויקט בינלאומי חדשני מפתח רובוט שיחקה תנועה של צמיחה ויסתגל לסביבה משתנה ובלתי צפויה – ממש כמו צמח


מחקר
פרויקט בינלאומי חדשני מפתח רובוט שיחקה תנועה של צמיחה ויסתגל לסביבה משתנה ובלתי צפויה – ממש כמו צמח

קבלת השראה מהטבע לפיתוחים טכנולוגיים אינה דבר יוצא דופן. כלי תעופה ששואבים השראה ממנגנוני התעופה של חרקים, ו"רובוטלף" המשתמש בסונאר ושואב השראה מיכולות הניווט של העטלפים, הם רק חלק מהפרויקטים המחקריים שמתבצעים באוניברסיטת תל אביב. עכשיו מוצע כיוון חדשני שמקבל השראה דווקא מעולם הצומח ומייצר חיבור מקורי במיוחד, שמותח את גבולות הדמיון מעלה והרחק מחוץ לקופסה, ממש כמו צמח מטפס. הרעיון המהפכני זיכה את החוקרים במענק של האיחוד האירופי ומתחיל לקרום עור וגידים בימים אלו ממש.
קבוצת מחקר מהפקולטה למדעי החיים ע"ש ג'ורג' ס.וייז באוניברסיטת תל אביב, בהובלת ד"ר יסמין מרוז, היא אחת מ-9 שותפות בפרויקט הבינתחומי והבינלאומי במסגרת תוכנית Horizon 2020 FET של האיחוד האירופי, התומכת בטכנולוגיות העתיד. הפרויקט עוסק בפיתוח רובוט שנקרא GrowBot, שמסוגל לטפס ולהתקדם בשטח באמצעות צמיחה, בהשראת צמחים מטפסים. הגישה החדשנית עשויה להוות פתרון מהפכני לאחד האתגרים המורכבים של תחום הרובוטיקה: תנועה בתנאים קשים, כשהשטח בלתי צפוי ואינו רציף. מובילת הפרויקט היא פרופ' ברברה מזוליי מהמכון האיטלקי לטכנולוגיה.
"רובוטים בעלי גלגלים או רגליים הקיימים היום, שרבים מהם פותחו בהשראת בעלי חיים, מסוגלים לנוע על פני משטחים, אך מתקשים להתמודד עם מכשולים – כמו מדרגות, סלעים, בקיעים ובורות," מסבירה ד"ר מרוז. "אנחנו מציעים גישה שונה לחלוטין: רובוט המבוסס על עולם הצומח. רובוט כזה, ששואב את השראתו מתנועת הגדילה של צמחים מטפסים – כמו הגפן, הקיסוס והזלזלת, יוכל להגיע כמעט לכל מקום: לטפס על סלעים ובניינים, לגשר על חללים ונחלים, וכך הלאה."
הפרויקט החדשני, במימון של 7 מיליון יורו, מקבץ יחדיו חוקרים מ-9 מעבדות ברחבי אירופה - באיטליה, בגרמניה, בישראל, בצרפת ובספרד, העוסקים במגוון רחב של תחומים: בוטניקה, רובוטיקה, מדע החומרים, מדעי המחשב, מתמטיקה, הנדסה, אנרגיה ועוד. מעבדתה של ד"ר מרוז תורמת את חלקה בתחום של התנהגות צמחים. "כן, יתכן שזה נשמע מפתיע, אך לצמחים יש מאפיינים התנהגותיים," היא אומרת. "צמחים מגיבים לסביבתם ומקבלים החלטות כל הזמן. אך מכיוון שבניגוד לבעלי חיים, צמחים הם נייחים, הם עושים דברים אחרת. בין היתר הם פותרים את בעיית התנועה באמצעות גדילה לכיוון המתאים: שולחים שורשים המותאמים למיקום המים, מטפסים ופונים לכיוונים שונים כדי להגיע לאור השמש, ועוד. צמחים מטפסים, שמהם אנו לומדים בפרויקט זה, מעגנים את עצמם בבליטות ובעצמים בדרכם למעלה, שומרים על משקל קל ומבנה דק, ויכולים להגיע לאורך של 200 מטר."
הרובוט הצומח יורכב מחומרים חדשניים, יגדל באמצעות שכפול עצמי, כמו בהדפסת תלת מימד, ויהיה קל ודק כמו צמח מטפס. מעבדתה של ד"ר מרוז אחראית על פיתוח מודלים מתמטיים שישולבו במוחו של הרובוט הצומח, ויאפשרו לו לעבד את המידע שיאסוף מהסביבה באמצעות מערכות חישה, ואחר כך לגבש החלטות נכונות ואסטרטגיית צמיחה אופטימלית, בהתאם לתוואי ולתנאי השטח.
"רובוט צומח יוכל לבצע משימות במקומות רבים שהם בלתי עבירים לאדם, לכלי רכב ולרובוטים בעלי רגליים וגלגלים; הוא יעבור מבעד לסדקים צרים, יטפס על סלעים וקירות, ויגשר על פני חללים," מסכמת ד"ר מרוז. "כך הוא יוכל לחדור להריסות של בניינים, לחקור את פני המאדים ואתרים ארכיאולוגיים, ולהיכנס לאתרים מזוהמים. כמו כן הוא עשוי להשתלב היטב בעיר החכמה של העתיד: מבנים רובוטיים שגדלים מעצמם יוכלו לשמש כגשרים, ואולי אף להפוך לבניינים שבונים את עצמם."

מחקר
מה יש לאבולוציה ללמד אותנו על רפואת שיניים? מומחית לננוטכנולוגיה ואורתודונטית-אנתרופולוגית מפתחות יחד חומרים וטיפולים חדשים כדי למנוע את את העששת של הדור הבא

על מה אתם חושבים כשאתם מדמיינים תור אצל רופא שיניים? אולי חלקינו היו חושבים על הרעש הלא נעים של המקדחה או על זריקת ההרדמה שמרגישה כמו "רק צביטה קטנה", אבל האם ידעתם שטיפול שיניים יכול להיות גם ביקור בחזית המדע? לא בכל בית ספר לרפואת שיניים יש מדען צמוד שעוסק בננוטנולוגיה ומפתח חומרים חדשים לשימוש רופאי השיניים, אף על פי שהשימוש בחומרים הנכונים הוא מרכיב חשוב של טיפולי שיניים כיום. בבית הספר לרפואת שיניים ע"ש גולדשלאגר באוניברסיטת תל אביב, ד"ר ליהי אדלר-אברמוביץ', מהמרכז לננטכנולוגיה, היא המומחית המקומית לחומרי ננו מאז שנת 2016.
הכל התחיל כשד"ר אדלר-אברמוביץ' הציגה את עבודתה בפגישה בה השתתפה ד"ר רחל שריג, אורתודונטית ואנתרופולוגית, אשר עשתה את התארים שלה ברפואת הפה בבית הספר לרפואת שיניים ואת הדוקטורט שלה באנטומיה ואנתרופולוגיה בפקולטה לרפואה ע"ש סאקלר. "כשראיתי את מה שליהי עובדת עליו, נדהמתי," מספרת ד"ר שריג, "ביליתי את כל חיי האקדמיים באוניברסיטת תל אביב. מיד ידעתי שהיא יכולה לעזור בפתרון הבעיות שאני נתקלת בהן כקלינאית."
ד"ר אדלר-אברמוביץ' מפתחת חומרים חדשים על מנת לשפר סתימות וכתרים, ואילו ד"ר רחל שריג עושה ניסויים על מנת לבדוק את העמידות והערך האנטי-בקטריאלי של החומרים. ד"ר אדלר-אברמוביץ' מרחיבה, "אני נהנית למצוא פתרונות לבעיות, ורחל תמיד כאן על מנת שאוכל לייצר חומרים על פי הצרכים הקליניים שלה, ולכוונן ולדייק אותם לפי המשוב שלה. במעבדה שלי לננוטכנולוגיה וחומרים ננו-ביולוגיים, אני גם יוצרת ננו-חומרים רפואיים, כגון הידרו-ג'לים כדי לייצר מחדש תאי עצם עבור רופאים בתחום הפריודונתיה ואורתופדיה. כדי להבין יותר טוב את מחלת בריחת הסידן – אוסטאופורוזיס – אני משתמשת בסימולטור שמדמה תנאים של היעדר כוח כבידה, כדי לבחון כיצד מיקרו-כבידה על גבי ספינות חלל משפיעה על צפיפות העצם ברמה התאית."
ד"ר שריג משתמשת במומחיות הננוטכנולוגית של ד"ר אדלר-אברמוביץ' גם כדי לחקור את התהליכים האבולוציוניים שעיצבו את הגולגולת ואת עצם הלסת של בני האדם. טכניקות ננוטכנולוגיות משמשות לניתוח מבני ומרקמי מיקרו, נוקשות, מורפולוגיה ותכולת פלואוריד של לסתות ושיניים, מהתקופה הפרהיסטורית ועד ימינו. ממצאי המחקר תורמים להבנת מקורותיהם של בעיות שיניים ולסת והקשר בין תזונה לבריאות הפה.
"למרות שיש לנו היגיינה טובה יותר וגישה לתרופות, רופאי השיניים רואים כיום יותר חורים וצפיפות שיניים," אומרת ד"ר שריג, האוצרת של האוספים לאנתרופולוגיה פיזית במכון לאנתרופולוגיה ע"ש משפחת שמוניס, במרכז דן דוד להתפתחות האדם ומחקר ביו-היסטורי, וכמו כן ראש המעבדה לאנתרופולוגיה של הפנים והשיניים בבית הספר לרפואת שיניים ע"ש גולדשלגר. "זה כנראה בגלל המעבר של בני האדם המוקדמים מציידים-לקטים לחקלאים, והשינויים התזונתיים שהגיעו יחד עם זה. הרפואה האבולוציונית עוזרת לנו לזהות מגמות כאלה, להבין את הפתולוגיות של היום ולפתח אסטרטגיות טיפול מוצלחות לבעיות כגון צפיפות שיניים, שיניים חסרות, חורים ומחלות חניכיים."
ואיך זה לעבוד ביחד? האם שותפות במחקר מתורגמת גם לחברות לא מדעית? "הפכנו לחברות לא רק בעבודה," מספרת ד"ר אדלר-אברמוביץ'. "אנחנו יודעות שנמשיך לעבוד ביחד – יש לנו כל כך הרבה רעיונות. מכיוון שבית הספר תומך בלימודי רפואת שיניים מעשיים כמו גם במחקר מדעי, שיתוף הפעולה שלנו הוא הרחבה טבעית של האווירה שלו. אנחנו תומכות אחת בשניה, אנחנו עובדות שעות מאוחרות, המעבדות שלנו אחת ליד השנייה, אנחנו חולקות ידע וציוד, אנחנו מגישות ביחד בקשות למענקי מחקר," אומרת ד"ר שריג. "תלמידי המחקר שלנו עובדים עם שתינו ולומדים כיצד לשתף פעולה וכיצד שילוב של מומחיות יכול ליצור משהו חדש."

מחקר
האם בקרוב התאים הלבנים שגורמים לאלרגיות יעזרו לנו לחסל את סרטן המעי הגס?

מה עושים עם תאי דם לבנים במערכת החיסונית שנותרו ללא עבודה ועושים יותר נזק מתועלת? רותמים אותם למלחמה במחלת הסרטן. החוקרות והחוקרים של אוניברסיטת תל אביב גילו במחקר ראשון מסוגו כי לאאוזינופילים, תאי דם לבנים של מערכת החיסון, יש יכולת להשמיד תאים ממאירים של סרטן המעי הגס - הסרטן השני בשכיחותו בישראל ואחד הקטלניים שבהם. הם מאמינים שהתגלית הזו יכולה להוביל לפיתוח טיפול במחלה.
אז איך מגלים שתאים שעיקר טיפולם הוא בכלל בזיהומים ובתולעי מעיים, יכולים לקטול תאים סרטניים? "אאוזינופילים הם תאי דם לבנים של מערכת החיסון, שמפרישים חלבוני הרס חזקים. תפקידם באבולוציה הוא להילחם בטפילים. אך בעולם המערבי המודרני, כשההיגיינה גבוהה והטפילים מעטים, הם הופכים תכופות לגורם שלילי, שמחולל אלרגיות ואסתמה" מסביר פרופ' מוניץ מהמחלקה למיקרוביולוגיה ואימונולוגיה קלינית בבית הספר לרפואה ע"ש סאקלר אוניברסיטת תל אביב, שבמעבדתו נערך המחקר פורץ הדרך.
פרופ' מוניץ והצוות שלו חיפשו דרך להפנות את כוחות-העל של האאוזינופילים הקטלניים למטרות טובות. "סברנו שיכולתם האגרסיבית של האאוזינופילים עשויה להוות גורם חיובי, במידה וההרס שהם זורעים מופנה כלפי תאים סרטניים. לכן ביקשנו לחקור את הקשר שלהם לסרטן – היבט שכמעט ולא נחקר עד היום". המחקר בוצע על ידי הדוקטורנטית הדר רייכמן ממעבדתו של פרופ' מוניץ, בשיתוף עם מחלקת הגסטרו בבית החולים איכילוב, והתפרסם לאחרונה בכתב העת Cancer Immunology Research.
לדברי פרופ' מוניץ, האאוזינופילים מרוכזים בעיקר ברקמות ריריות בגוף שבאות במגע עם העולם החיצון, כמו מערכת הנשימה, מערכת העיכול ומערכות השתן והמין. המאגר הגדול ביותר שלהם מצוי במערכת העיכול, ולכן החליטו החוקרים להתרכז בסרטן המעי הגס.
בשלב הראשון הם נטלו דגימות מגידולים של 275 חולים, ובדקו אם יש קשר בין מספר האאוזינופילים בגידול לבין דרגת החומרה של המחלה. "גילינו שככל שיש בגידול יותר אאוזינופילים, כך פוחתת חומרת המחלה", אומר פרופ' מוניץ ומסביר "כעת, כדי לברר אם משמעות הדבר היא שהאאוזינופילים נלחמים ופוגעים בסרטן, חקרנו מודלים שונים של סרטן המעי הגס בעכברים".
"ראשית מצאנו שהסביבה הסרטנית מזמינה אליה את התאים הללו, והם מסוגלים ממש להסתנן לתוך הגידולים ואף לחיות בתוכם במשך זמן רב. גילינו גם שעכברים שהונדסו כך שאין להם כלל אאוזינופילים, פיתחו מספר גדול בהרבה של גידולים מעכברים בעלי אאוזינופילים, ומתו תוך זמן קצר יותר ולהיפך. מסקנתנו מהניסוי הייתה שלאאוזינופילים יש תפקיד בבלימת התקדמותו של סרטן המעי הגס".
אאוזינופילים בדרך לאתר נגוע
בשלב הבא של המחקר נלקחו אאוזינופילים מבני אדם ומעכברים והוכנסו למבחנות יחד עם דגימות של תאים סרטניים. בשלב זה התברר שהנחת המחקר הייתה נכונה - האאוזינופילים אכן הצליחו להשמיד את תאי הסרטן. החוקרים גילו עוד משהו מעניין – שניתן לזהות אאוזינופילים שנלקחו מגידולים סרטניים בעזרת חתימה גנטית ייחודית, המעידה על פעילות מוגברת.
"המשמעות היא, ככל הנראה, שהאאוזינופילים הנמצאים בגידול מגיבים לחומרים הנמצאים בסביבתם, ואלו גורמים להם להפריש כמות גדולה במיוחד של חלבונים המסוגלים להרוג תאי סרטן", אומר פרופ' מוניץ. "באנליזה מדוקדקת של האאוזינופילים גילינו שהם מגיבים במיוחד לחלבון בשם אינטרפרון גמא, והסקנו שהוא כנראה האחראי להגברת פעילותם. ואכן, הוספת אינטרפרון גמא למבחנות העצימה מאוד את פעילות ההרג של האאוזינופילים אל מול התאים הסרטניים".
בישראל מאובחנים מדי שנה כ-3,200 חולות וחולים בסרטן המעי הגס, ופרופ' מוניץ מקווה שבעזרת התגלית החדשה העתיד שלהם יהיה אופטימי יותר. "למעשה גילינו יעד חדש לטיפולי אימונותרפיה לחולי סרטן בעזרת האאוזינופילים. אנחנו מקווים שהמחקר שלנו ישמש תשתית לפיתוח תרופות במספר גישות שונות: חומרים שיגייסו יותר אאוזינופילים אל סביבת הגידול, חומרים שיגבירו את פעילותם של האאוזינופילים שכבר נמצאים בסביבת הגידול, וכן טיפולים משולבים שיחברו בין אאוזינופילים לתאי T, ובכך יחזקו את יעילות הטיפול. במעבדה שלי אנחנו עובדים כעת על כל ההיבטים הללו, ומנסים, בין היתר, לזהות את החלבון המסוים המופרש על ידי האאוזינופילים, שהורג את הסרטן".
"כמובן שהמחקר הזה פתח בפנינו עולם שלם ונסתר שהיינו מעוניינים לצלול לתוכו ולחקור. לדוגמא: האם אאוזינופילים מסוגלים גם להרוג סוגי סרטן שונים? מהם המנגנונים שמבקרים את פעילותם? האם הם מתנהגים באופן דומה כנגד כל סוגי הסרטן או רק נגד סוגי סרטן ספציפיים? מה מאפיין את החולים שיש להם אאוזינופילים בגידול לעומת אלו שאין להם? האם אנחנו מסוגלים לרתום את האאוזינופילים בכדי להילחם בגידולים כאסטרטגיה טיפולית?"
לשאלה על השינויים העתידיים בתחום המחקר עונה פרופ' מוניץ: "אני חושב שאנחנו נמצאים בעידן מרתק מבחינת התפתחות הרפואה. זהו עידן בו הטכנולוגיה פוגשת אותנו בכל מקום, ואחד הממשקים המשמעותיים ביותר למפגש שכזה הוא עולם הרפואה. היום ישנה הבנה כי מחלות שבעבר הגדרנו כ״יישות״ אחת עשויות להתנהג באופן שונה לגמרי אצל כל אחד. הדבר הזה מעורר את הצורך להבין מצד אחד את ההטרוגניות של מחלות, ומצד שני להבין כי כוחן של תרופות ״גנריות״ שאינן מותאמות אישית, הוא מוגבל".
"בעתיד אנחנו נראה שיטות מגוונות, בהן ריצוף גנטי, איפיון המיקרוביום ועוד לפילוח אוכלוסיות של חולים, אשר יאפשר לרופאים להתאים תרופות באופן פרטני. בנוסף, אני מעריך כי בעתיד יהיו טכנולוגיות אשר יאפשרו זיהוי מוקדם של מחלות ומניעתן מבעוד מועד על ידי סריקה של סמנים ביולוגיים שונים. אני סבור כי יושקעו מאמצים ב״חינוך״ הציבור והרופאים לנצל טכנולוגיות שכבר קיימות על מנת לזהות מחלות בשלב מוקדם יותר או חינוך לאורח חיים בריא יותר".
"החלום שלי הוא שנצליח לפתח טיפול לחולי סרטן אשר מבוסס בעיקרו על גיוסם של אאוזינופילים לסביבה הסרטנית וניצול היכולות שלהם להרוג תאי סרטניים," מסכם פרופ' מוניץ.

מחקר
ניסויים שנעשו על שמרים יהיו בסיס לפיתוח תרופות למחלות מטבוליות תורשתיות

הם מוכרים לכולנו בעיקר מעולם האפייה ומשמשים גם לייצור משקאות אלכוהוליים, אבל האם ידעתם שהשמרים חולקים עם האדם חלק ניכר מהגנום? שמרים הם פטריות חד-תאיות, המפיקות את האנרגיה שלהן על ידי פירוק סוכר המצוי בסביבתן. חוץ מזה, הם משמשים כבר שנים רבות למחקר. בעזרתם גילו חוקרים באוניברסיטת תל אביב ממש לאחרונה פתרון מפתיע ופורץ דרך, שעשוי לסלול את הדרך לתרופה למחלות מטבוליות, הפוגעות בחילוף החומרים בגוף.
לכל יילוד בישראל נערכות בדיקות לגילוי של מחלות מטבוליות, מכיוון שרק גילוי מוקדם יכול למנוע נזק חמור. נכון להיום, לחלק ניכר מהמחלות הללו אין טיפול יעיל, והחולים חייבים להימנע כל חייהם מצריכת מזונות המכילים את החומר שגופם אינו מסוגל לפרק. בהיעדר טיפול, גורמות המחלות הללו לתופעות חמורות ביותר כמו פגיעה רב-מערכתית, התדרדרות נוירולוגית, פרכוסים, מוגבלות שכלית ולעתים אף אוטיזם. הטיפול העיקרי המוכר כיום הוא דיאטה חריפה, שקשה מאוד לעמוד בה כל החיים.
"במחלות מטבוליות נפגע גן האחראי על ייצור אנזים שמפרק מטבוליט מסוים (חומר המשתתף בתהליכי חילוף החומרים בגוף)," מסביר פרופ' אהוד גזית מהמחלקה למיקרוביולוגיה מולקולרית וביוטכנולוגיה בפקולטה למדעי החיים ע"ש ג'ורג' ס.וייז באוניברסיטת תל אביב. "בהיעדר האנזים מצטברות בגוף כמויות גדולות של אותו מטבוליט, והצטברותו מובילה ליצירת מבנים עמילואידים שעלולים לגרום לנזקים קשים. כבר זמן רב ידוע שהעמילואידים, מבנים חלבוניים שנוצרים בתהליך של הרכבה עצמית, קשורים למחלות קשות של מערכת העצבים המרכזית, כמו אלצהיימר, פרקינסון, ALS והנטינגטון. ניסויים קודמים במעבדה שלנו הוכיחו שהם מאפיינים גם מחלות מטבוליות גנטיות."
כהמשך לממצאים קודמים במעבדתו של פרופ' גזית, שבהם נבדקו מבני העמילואידים בתוך מבחנות במעבדה, ביקשו החוקרים לבחון את הצטברות העמילואידים בתוך תא חי. לשם כך הם פיתחו מערכת מחקר חדשנית על מודל של שמרים, שמטרתה לחקור את המנגנונים של מחלות מטבוליות תורשתיות, בהן: פנילקטונוריה, טירוזינמיה, מחלת סירופ מייפל – MSUD, הומוציסטינוריה ועוד, ולפתח עבורן תרופות. המחקר פורץ הדרך הובל על ידי ד"ר דנה לאור ממעבדתו של פרופ' גזית, בשיתוף עם מרכז בלווטניק לפיתוח תרופות, והתפרסם בכתב העת Nature Communications.
"למודלים שמריים מסוג זה יש יתרונות רבים במחקר, והם אף עומדים מאחורי שלושה פרסי נובל רק בעשור האחרון!" מדגישה ד"ר לאור, "אנחנו בחרנו בהם כי הם מאפשרים לנו לבצע מניפולציות גנטיות באופן זריז, יעיל ואמין, ובנוסף, הם שימרו לאורך האבולוציה מסלולים מטבוליים חיוניים, שקיימים בכל היצורים החיים, וכמובן גם באדם."
החוקרים יצרו מוטציה במערכת השמרית בגנים האחראים על ייצור אנזימים, שמפרקים מטבוליט חיוני בשם אדנין. בהיעדר האנזימים המפרקים, הצטברו בתא השמר מולקולות של אדנין, שהתקבצו יחדיו למבנים עמילואידיים, וגרמו למותו של התא.
"בדקנו שמרים עם רמות שונות של אדנין," מתארת ד"ר לאור. "גילינו שעד רמה מסוימת, האדנין אינו הורג את התא, ואז בבת אחת, כשהוא עובר רמה מסוימת, התא מת. ההסבר לכך הוא שדרושה רמה מסוימת של אדנין כדי להניע תהליך של הרכבה עצמית, שבו נוצרים מבנים עמילואידיים. מסתבר שהמבנים הללו – ולא האדנין כשלעצמו – הם שהורגים את התא."
בשלב הבא הוסיפו החוקרים למערכת חומצה טאנית, חומר טבעי המופק מצמחים, שידוע כי הוא מעכב את היווצרות העמילואידים. ואכן, המבנים הרעילים לא נוצרו, ותמותת תאי השמר נמנעה. בעקבות הממצאים המעודדים, החוקרים מאמינים שעבודתם עשויה לשמש בסיס לפיתוח תרופות יעילות ונגישות למחלות הגנטיות הקשות.
"המחקר שלנו יכול לשמש כבסיס לפיתוח תרופות למחלות מטבוליות תורשתיות ונדירות שגורמות סבל רב לחולים, ולרובן אין כיום פתרון זמין ונוח," מסכמת ד"ר לאור. "כל מחלה לכשעצמה נדירה, אך ביחד הן מהוות חלק ניכר מכלל החולים במחלות גנטיות מולדות. במקום דיאטה קיצונית לכל החיים, אנחנו מבקשים לפתח תרופות וטיפולים נגישים. בעקבות הצלחת המחקר הראשון במודל שמרי, הגשנו פטנט לרישום, והצלחנו לגייס מימון מטעם האוניברסיטה על מנת להמשיך בפיתוח הטכנולוגיה. כיום אנחנו ממשיכים לפתח מודלים שמריים עם מוטציות למחלות מטבוליות נוספות, ולהיעזר בהם כדי לנסות לגלות תרופות פוטנציאליות, שיוכלו לשפר ללא הכר את איכות חייהם של החולים, ואף להציל חיים."

מחקר
אסטרונומים מאוניברסיטת תל אביב זיהו תופעה בלתי מוכרת המזינה ומגדילה חורים שחורים ענקיים במהירות רבה

מי מאיתנו לא חש לעתים צורך עז לפשוט על המקרר ולאכול מכל הבא ליד? מסתבר שגם לחורים שחורים יש לפעמים תחושת רעב בלתי מוסברת. ההבדל בינינו לבינם הוא שאנחנו במקרה הגרוע ניאלץ לעבור לחור הבא בחגורה, ואילו הם יגדלו במהירות למסות שכבדות פי מיליארד מהשמש שלנו. קבוצת חוקרים מאוניברסיטת תל אביב גילתה לאחרונה מנגנון חדש ובלתי מוכר האחראי לגדילה המפלצתית של חורי ענק שחורים.
חורים שחורים הם תופעה מוכרת. התצפיות עליהם מגלות לנו שהם מצויים בכל גלקסיה, ושקצב גידולם הוא לרוב איטי ומתמשך. אבל לאחרונה זיהו אסטרונומים תופעה מעניינת: חורים שגדלים למידדים מפלצתיים תוך חודשים ספורים.
"חורים שחורים ענקיים, שכבדים פי מיליון ועד פי מיליארד מהשמש שלנו, שוכנים במרכזן של רוב הגלקסיות ביקום," מסביר ד"ר טרכטנברוט, שיחד עם ד"ר יאיר הרכבי וקבוצת החוקרים שלהם מהחוג לאסטרופיזיקה בבית הספר לפיזיקה ולאסטרונומיה ע"ש ריימונד ובברלי סאקלר גילו מנגנון חדש לחלוטין, האחראי לגדילה מואצת של חורי ענק שחורים.
"במרכז גלקסיית שביל החלב שבה אנחנו חיים למשל, שוכן חור שחור ענק בעל מסה של 4 מיליון מסות שמש. למרות שכיחותם, עד היום עדיין לא היה ברור כיצד חורים שחורים כאלו גדלים למסות כל כך גדולות. ייתכן שהממצאים החדשים יכולים להסביר איך זה קורה". מחקרם המשותף עם פרופ' חגי נצר, גם הוא מהחוג לאסטרופיזיקה, יחד עם צוות חוקרים מרחבי העולם (ארה"ב, צ'ילה, פולין ואנגליה) התפרסם בכתב העת Nature Astronomy.
"בעבר זוהו מספר אירועים דרמטיים בהם חורים שחורים 'בולעים' כוכב או חומר אחר הנמצא בסביבתם, וגדלים בדרך זו", מסביר ד"ר הרכבי ומוסיף "כשצפינו באירוע האסטרונומי בעל השם הקליט AT 2017bgt, שנצפה בשנת 2017, נתנו תחילה גם לו את הפרשנות הזו, אך נתונים שונים גרמו לנו לחשוד שהפעם מדובר בתהליך שונה ובלתי מוכר" .
החוקרים עקבו אחר האירוע במשך למעלה משנה בעזרת טלסקופים שונים, על הקרקע ובחלל, כולל הטלסקופ החדש NICER, שמותקן בתחנת החלל הבינלאומית, והטלסקופ האולטרה-סגול שעל גבי הלוויין Swift, וביססו את ההנחה שהוא אינו דומה לשום דבר שנצפה בעבר.
הרמז הראשון לחריגותו של האירוע היה רכיב אור נוסף, שנראה כמעין קווי פליטה עשויים יוני חמצן, חנקן והליום, ואינו אופייני לאירועים מוכרים של בליעת כוכבים. תצפיות אלה של החוקרים תאמו לתחזיות תיאורטיות של פרופ' נצר. "עוד בשנות ה-80 חזינו תהליך שבו חור שחור בולע גז שנמצא בסביבתו ויכול להוביל לרכיבי האור שנצפו. המחקר החדש מהווה את הגילוי הראשון של התהליך בפועל," מסביר נצר.
עוד הם גילו כי עוצמת הקרינה הבוקעת מסביבת החור השחור גדלה פי יותר מ-50 בתוך זמן קצר ביותר - ככל הנראה חודשים ספורים בלבד.
לאחרונה זיהתה קבוצת החוקרים שני אירועים נוספים בהם חורים שחורים נראים כ"נדלקים", תוך שהם פולטים אור באופן דומה לזה שנצפה באירוע AT 2017bgt. שלושת האירועים מהווים סוג חדש ומסקרן של 'הזנה' מואצת של חורים שחורים, באופן שלא היה מוכר קודם.
"אנחנו עדיין לא בטוחים מה גורם לחורים השחורים האלה להאיץ את קצב הגידול שלהם באופן דרמטי ופתאומי כל כך", אומר ד"ר טרכטנברוט. "ישנם מנגנונים רבים להאצת קצב הגידול של חורים שחורים, אבל רובם מתרחשים על פני תקופות ארוכות הרבה יותר".
כעת משיקים החוקרים פרויקט שמטרתו לגלות עוד אירועים כאלו ולעקוב אחריהם בעזרת מספר רב של טלסקופים. "רק כך נוכל למפות את מכלול הדרכים בהן חורים שחורים בולעים חומר, להבין מה מעורר אותם לעשות זאת ואולי לפתור סוף סוף את חידת היווצרותן של 'המפלצות' האלה, השוכנות במרכזי גלקסיות״, מסכם ד"ר הרכבי.

מחקר
חוקרים באוניברסיטת תל אביב זיהו חלבון המתריע על התפתחותם של גידולים סרטניים בגוף

כולנו יודעים עד כמה חשוב להיזהר מווירוסים ומחיידקים המאיימים על בריאותנו. תחום הרפואה כבר הצטייד במגוון כלים יעילים להדוף חלק גדול מגורמי המחלות האלו, על ידי חיסונים, אנטיביוטיקה ועוד. אך בשנים האחרונות חוקרים מפנים את הזרקור אל הגנום שלנו, שיש לו תפקיד מהותי בשמירה על בריאותנו, ומצביעים על כך שגם היציבות של ה-DNA שלנו יכולה להתערער. "אנחנו יודעים היום שה-DNA בתאי גופנו מותקף וניזוק ללא הרף על ידי מגוון גורמים: גורמים חיצוניים, כגון קרינה, כימיקלים המזהמים את סביבתנו, סוגי מזון מסוימים ועישון, וגם רדיקלים חמצניים הנוצרים ללא הרף בתוך התא." מסביר פרופ' יוסי שילה מהמחלקה לגנטיקה מולקולרית של האדם ולביוכימיה בפקולטה לרפואה ע"ש סאקלר.
"פגיעות אלה ב-DNA הן גורם מרכזי למחלות רבות ושונות, בהן הסרטן לסוגיו, מגוון מחלות כרוניות נפוצות ואף הזדקנות מואצת. מדוע וכיצד, אם כן, רובנו נותרים בריאים רוב הזמן? זאת, בזכות מנגנוני ההגנה המתוחכמים המופעלים בתא הבריא, העסוקים ללא הרף בתיקון הנזקים ב- ,DNA או במילים אחרות, שומרים על יציבות הגנום."
פרופ' שילה משווה את מנגנוני ההגנה הללו לצבא: קיים צבא סדיר מצומצם, המונה עשרות חלבונים חרוצים, שכל תפקידם לתקן נזקים ל-DNA, ולצדו צבא מילואים של מאות חלבונים בעלי תפקידים שונים במרחבי התא, המגויסים למשימה בעתות חירום – לדוגמה כאשר נגרם קרע ב-DNA.
בשנת 1995 התגלה במעבדתו של פרופ' שילה החלבון שאחראי על אותו "צו שמונה" שמקפיץ לפעולה את הצבא הסדיר ואת "כוחות המילואים" שחשים לעזרתו, חלבון ששמו ATM. "מאז אנחנו חוקרים את עיקרון הפעולה של ATM, ואת האופן בו הוא מגייס לפעולה את ה'חיילים' השונים מכל רחבי התא, ואף גילינו מספר מגויסים כאלה," הוא אומר.
לאחרונה, באמצעות סריקה רחבת היקף של חלבוני התא, גילו החוקרים מגויס חדש למערכת - חלבון בשם יוביקווילין 4. "עד עתה היה ידוע שיוביקווילין 4 מסייע בפירוק חלבונים בתא, לאו דווקא בהקשר של יציבות הגנום. והנה, זיהינו אותו כעוד אחד מפקודיו של ATM במערך לתיקון קרעים ב-DNA," מספר פרופ' שילה.
המחקר בוצע במעבדתו של פרופ' שילה על ידי ד"ר רון יחימוביץ, ד"ר יעל זיו והדוקטורנטית בהוואנה ולפולה, בשיתוף עם מעבדתו של פרופ' כריסטיאן ריינהרדט מאוניברסיטת קלן בגרמניה, והתפרסם בכתב העת היוקרתי Cell.
בשל הקשר ההדוק שבין יציבות הגנום להופעת סרטן, החוקרים השוו את רמת החלבון יוביקווילין 4 בדגימות מגידולים ממאירים, לעומת רקמות בריאות שנלקחו מאותם חולים. החוקרים מצאו שבחלק מהמקרים, כמות היוביקווילין 4 בתאי הגידול הייתה גבוהה באופן משמעותי בהשוואה לתאים בריאים מאותו חולה.
בירור נוסף העלה, שהגידולים שבהם נצפתה רמה גבוהה מהנורמלית של יוביקווילין 4, מצויים בשלב המתקדם של המחלה. אלה הגידולים שהגיעו לשלב האגרסיבי, שהוא בעל פוטנציאל ליצור גרורות, ובנוסף לכך – הם בעלי עמידות גבוהה יותר לטיפולים כימותרפיים מסוימים, וכן לטיפולי הקרנה.
"מהממצאים הבנו כי אף על פי שיוביקווילין 4 משתתף בשמירת יציבות הגנום, כמות מוגברת שלו דווקא מערערת את מנגנון התגובה לנזקי DNA, הבנוי על בלמים ואיזונים עדינים ומדויקים," מסביר פרופ' שילה. "במצב כזה, מסתבר, יוביקווילין 4 דווקא תומך בהתפתחות הסרטן, ואף פוגע ביעילותם של טיפולים מקובלים. עם זאת, התברר, כי גידולים כאלה עתידים להגיב טוב יותר לטיפולים כימותרפיים אחרים, שדווקא הופכים ליעילים יותר בתאים בעלי רמה גבוהה של החלבון."
לממצא זה חשיבות גדולה ברמה הקלינית: החוקרים סבורים, כי ליוביקווילין 4 פוטנציאל מבטיח לשמש כמדד אונקולוגי רב-ערך, המעיד מחד גיסא על מצבו של החולה ועל מידת התקדמות הגידול בעת אבחונו, ומאידך גיסא - מסייע לרופא לקבוע עבור החולה את הטיפול המתאים. בכך נותן המחקר מענה לאחד האתגרים המרכזיים בחקר הסרטן כיום: יצירת סמנים ביולוגיים שיסייעו בסיווגן של ממאירויות ובתכנון הטיפול המתאים, ברמה האישית.
"ממצאינו מעידים, שהגן המכתיב את ייצורו של יוביקווילין 4 עשוי להיות אונקוגן חדש – גן שכאשר פעילותו מוגברת, וכמות החלבון המוכתב על ידו עולה - מואץ התהליך הסרטני," מסכם פרופ' שילה. "כיום, ממשיכה מעבדתנו בשיתוף פעולה עם קבוצתו של פרופ' ריינהרדט, לחקור את תפקידיו של יוביקווילין 4, בעיקר בעת שהוא משמש כחייל מילואים במערך המסועף השומר על יציבות הגנום. במקביל, אנו מרחיבים את קשת המחלות הממאירות שבהן אנו בוחנים את רמתו. כל זאת, במקביל להמשך החיפוש אחר 'חיילים' נוספים המגויסים על ידי ATM למערך תיקון נזקים בגנום. מספרם נאמד במאות רבות, ולכן למחקר זה נכונו עתידות."

מחקר
בעקבות הממצאים המדאיגים, החוקרים קוראים לציבור להפחית את השימוש במוצרי פלסטיק ובמוצרים חד פעמיים

זיהומי פלסטיק בים והנזק שהם גורמים לסביבה הימית בכלל ולבעלי חיים ימיים בפרט הם נושא עכשווי בוער ביותר בתחום ההגנה על הטבע, ויום איכות הסביבה העולמי (5.6.18) אף הוקדש השנה לנושא זה. ואכן, על פי נתוני המשרד להגנת הסביבה, משתמשים בני האדם בכמויות עצומות של פלסטיק: בכל דקה נרכשים בעולם כמיליון בקבוקי שתייה מפלסטיק, ו-500 מיליארד שקיות פלסטיק נצרכות מדי שנה. חלק גדול מהפלסטיק שאנו צורכים, כ-8 מיליון טון בשנה, מגיע אל האוקיינוסים – שווה ערך למשאית עמוסה הנשפכת לים בכל דקה. ועוד: הערכות עדכניות קובעות כי כ-80% מכל הזיהום הימי כיום מקורו במוצרי פלסטיק.
במחקר שנערך במעבדתה של פרופ' נועה שנקר מבית הספר לזואולוגיה של אוניברסיטת תל אביב ומוזיאון הטבע ע"ש שטיינהרדט נדגמו חסרי חוליות מסוג איצטלנים מתשעה אתרים לאורך חופי ישראל, בים התיכון ובמפרץ אילת. בדגימות מכל החופים נמצאו בגופם של האיצטלנים חלקיקי מיקרו-פלסטיק שגודלם קטן מחמישה מילימטרים, ובבעלי חיים ממי חופים רבים נמצאו גם כימיקלים מסוג פתאלטים, שמשמשים את תעשיית הפלסטיק ועלולים לגרום למגוון נזקים כולל שיבושים הורמונליים. המחקר, בהובלת הדוקטורנטית גל ורד מבית הספר לזואולוגיה, ובשיתוף פרופ' דרור אבישר ואביב קפלן מבית הספר לסביבה ומדעי כדור הארץ ע"ש פורטר, התפרסם בכתב העת Marine Pollution Bulletin.
"בסביבה הימית מתפרקים מוצרי הפלסטיק לחלקיקים זעירים המכונים מיקרו-פלסטיק, שגודלם נע מכמה עשרות מיקרונים (מיקרון = מיליונית המטר) ועד חמישה מילימטרים, כך שאת רובם לא ניתן לראותם בעין," מסבירה פרופ' שנקר. "בנוסף, הם משחררים למים כימיקלים שונים המשמשים את תעשיית הפלסטיק להקניית מגוון תכונות למוצריה – כמו גמישות, חוזק, צבע ועוד, אך עלולים לגרום נזקים שונים וקשים ליצורים חיים, כמו למשל שיבושים הורמונליים. אנחנו ביקשנו לבחון את רמת זיהום הפלסטיק שמגיעה לחיות ימיות לאורך חופי ישראל, ומכאן להסיק לגבי חומרת הזיהום במים."
לראשונה בעולם במחקר מסוג זה נעזרו החוקרים בבעל חיים חסר חוליות בשם איצטלן, שנפוץ בכל בתי הגידול הימיים בעולם, ומתאים במיוחד למחקר מסוג זה: זהו בעל חיים ישיב שנצמד לסלע ואינו זז ממקומו כל ימי חייו. הוא ניזון על ידי סינון של עשרות ליטרים של מי ים מדי יום, וכשהמים מזוהמים, מצטברים בגופו גם המזהמים. לכן בדיקה של איצטלנים שנלקחו מחוף מסוים נותנת תמונה אמינה ביותר על מצב הזיהום ורמת הבריאות הסביבתית באותו אתר. במונחים מדעיים מהווים האיצטלנים סמנים ביולוגיים של איכות הסביבה הימית. בנוסף, קבוצה זו של חסרי חוליות היא הקרובה ביותר מבחינה אבולוציונית לחולייתנים (דוגמת בני האדם), ולכן היא מהווה מערכת מודל נפוצה למחקר.

פסולת פלסטיק על גבי מלפפון ים בשונית האלמוגים באילת (צילום: גיארמו בן-נעים אנדרסון)
לצורך המחקר דגמו החוקרים איצטלנים מתשעה אתרים שונים, בהם נמלים, חופי רחצה ושמורות טבע. שבעה מהאתרים פרוסים לאורך חוף הים התיכון, מצפון עד דרום: שמורת אכזיב, נמל עכו, מכמורת, הרצליה, בת ים, הפארק הלאומי פלמחים והפארק הלאומי אשקלון; ושניים נמצאים בים סוף: המרינה באילת וריף הדולפינים. לאחר מכן הם בדקו במעבדה את כמות חלקיקי המיקרו-פלסטיק בכל פרט; בנוסף, באמצעות שיטת אנליזה כימית חדשה ומדויקת ביותר, שפותחה במרכז לחקר המים בראשות פרופ' אבישר, הם חיפשו באיצטלנים שרידים של תוספי פלסטיק מסוג פתאלטים המעניקים גמישות למוצרים, ועלולים לגרום לשיבושים הורמונליים ולמגוון נזקים אחרים אצל בעלי חיים ובני אדם. והתוצאות צריכות להדאיג את כולנו.
"בכל האתרים שבדקנו מצאנו איצטלנים עם חלקיקי מיקרו-פלסטיק, ובמרבית האתרים מצאנו גם תוספים תעשייתיים מסוג פתאלטים," אומרת החוקרת גל ורד. "חשוב לציין שלא תמיד נמצא קשר ברור בין ייעודו של החוף (נמל, חוף רחצה, פארק לאומי), ורמת הזיהום הגלויה לעין, לבין הממצאים שלנו. לדוגמה: בהשוואה בין שני חופי רחצה קרובים, בעלי רמת ניקיון דומה לכאורה, נמצא באחד ריכוז גבוה של פתאלטים, בעוד שבשני כמעט שלא היו פתאלטים כלל. ריף הדולפינים באילת הצטיין בהיעדר כמעט מוחלט של תוספי פלסטיק, אך לעומת זאת, הצטערנו לגלות רמות גבוהות של תוספי פלסטיק בחופי רחצה שרבים מאיתנו נוהגים לפקוד עם ילדינו."
"המחקר שלנו מדליק נורה אדומה לכל הציבור בישראל," מסכמת פרופ' שנקר. "גם אם לא תמיד ניתן לראות זאת בעין, הממצאים מראים שהחופים שלנו מזוהמים במיקרו-פלסטיק ובכימיקלים שמקורם במוצרי פלסטיק. פלסטיק הוא חומר שיצר האדם לשימושו, והוא נמצא בשימוש רחב ביותר, אך הוא יכול להיות מסוכן לסביבה וגם לנו. לכן כולנו מחויבים להשתמש בו באחריות. בנוסף למיחזור בקבוקים ואריזות, אנחנו קוראים לציבור, בין היתר, להפחית את השימוש במוצרי פלסטיק ובפרט במוצרים חד פעמיים. זה בידיים שלנו!"

מחקר
אצות שגודלו במי מלח יצילו את העולם ממגפת הפלסטיק

פלסטיק מתכלה הוא העתיד. היינו שמחים לו בקבוק הפלסטיק שהבאנו אתמול מהסופר ישמיד את עצמו עד תום קריאת כתבה זו, אבל אנחנו עדיין לא שם. נכון להיום, פלסטיק מתכלה נשאר בסביבה שלנו כמה חודשים עד כמה שנים. אמנם זה שיפור משמעותי על פני פלסטיק "רגיל", שמתכלה רק לאחר אלפי שנים, אך לפלסטיק מתכלה יש גם חסרון בולט נוסף - עד היום כדי לייצר פלסטיק כזה צריך היה להשקיע כמות עצומה של מים מתוקים בתהליך הייצור. מים מתוקים הם משאב יקר, וגם ההתחממות הגלובלית מביאה אותנו להבנה שאין לנו מים לבזבז. אז מה עושים? חוקרים מאוניברסיטת תל אביב הצליחו להתגבר על הבעיה, והפיקו פולימר פלסטיק ממיקרואורגניזמים קדומים ומאצות שגודלו במי ים.
ידידותי לסביבה אך בזבזני במשאבים
פלסטיק הוא אחד המזהמים הבעייתיים והנפוצים בעולם. מדובר בפולימר המופק מתוצרי נפט לשימוש תעשייתי, אשר עיבודו משחרר מזהמים כימיים כתוצר לוואי. החיים המודרניים מעודדים אותנו לצרוך עוד ועוד מוצרים שעשויים או ארוזים בפלסטיק, שנזרק אחרי שימוש קצר אבל לא נעלם. לא פעם אנו נחשפים בשידורי החדשות למראה הסוריאליסטי של איי פלסטיק באוקיינוסים, העשויים מבקבוקים, אריזות ושקיות, מזהמים את הסביבה ומהווים סכנה לבעלי החיים.
הפתרון למגפת הפלסטיק אותו מיישמים היום הוא הביו-פלסטיק: פלסטיק המיוצר מביו-פולימרים כמו צמחים או חיידקים, שאינו מצריך נפט ומתכלה במהרה. זה נשמע טוב, ויש כבר מפעלים רבים שמייצרים פלסטיק ביולוגי מסוג זה בכמויות מסחריות, אבל מסתבר שגם לשימוש בביו-פולימרים יש מחיר: כדי לגדל את הצמחים ואת החיידקים שמשמשים להכנתו יש צורך בשטחי קרקע פורייה ובמים מתוקים לרוב, אשר נחשבים למשאבים מוגבלים ויקרים. לכן המעבר לביו-פלסטיק נחשב עדיין בעייתי ולא משתלם במדינות עניות במים כמו ישראל.
במחקר רב-תחומי בהובלת ד"ר אלכסנדר גולברג מבית הספר לסביבה ולמדעי כדור הארץ ע"ש פורטר, ופרופ' מיכאל גוזין מבית הספר לכימיה, הצליחו החוקרים להפיק ביו-פולימרים בתהליך שאינו דורש קרקע חקלאית או מים מתוקים. תוצאות המחקר המהפכני התפרסמו בכתב העת היוקרתי Bioresource Technology.

נפלטו יחד מהמים. בעלי חיים ופסולת על חוף הים
להחזיר את גלגל הזיהום של כדור הארץ לאחור
"חומר הגלם בו השתמשנו ליצירת הפלסטיק הביולוגי היה אצות רב-תאיות שגדלות בים", מסביר ד"ר גולברג. "האצות אכלו ארכאונים חד-תאיים (מיקרו-אורגניזמים חסרי גרעין ואברונים), שגם הם גדלים במים מלוחים מאוד. לאחר מכן הן תססו ויצרו את הפולימרים הביולוגים. מדובר בפריצת דרך משמעותית. התהליך שאנחנו מציעים יאפשר גם למדינות הסובלות ממחסור במים מתוקים, כמו ישראל, סין והודו, לעבור לפלסטיק מתכלה".
לדברי ד"ר גולברג, המחקר החדש יכול לחולל מהפכה בהורדת נטל הפלסטיק מהסביבה: "פלסטיק ממקורות מאובנים מהווה את אחד הגורמים המזהמים ביותר באוקיינוסים. מצד שני, תהליך הייצור של פלסטיקים מתכלים מצריך משאבים חשובים, שגם הם הולכים ומתמעטים. מדינה כמו ישראל, שהיא צרכנית פלסטיק גדולה, לא תקצה שטחים נרחבים ומים יקרים כדי לייצר ביו-פולימרים. במחקר שלנו הצלחנו להוכיח לראשונה שאפשר לייצר ביו-פלסטיק בתהליך שהוא ידידותי גם לסביבה וגם לתושבים".
בימים אלה עובדים החוקרים על דיוק שיטתם באמצעות שימוש בחיידקים שונים ובאצות שונות להפקת הפלסטיק. "כרגע אנחנו מנסים להבין כיצד זנים שונים של חיידקים מביאים לתסיסה שונה בקרב מינים שונים של אצות", אומר ד"ר גולברג. "כל אצה מייצרת סוכר שונה, כך שתוצר הפלסטיק הסופי גם הוא שונה. המטרה שלנו כעת היא למצוא את החיידקים ואת האצות המתאימים ביותר להפקת פולימרים לפלסטיקים".

מחקר
בשיטה חסרת תקדים הצליחו החוקרים למדוד מסה של חור שחור, לפי תנועת ענני הגז סביבו

בשנים האחרונות, מנסים חוקרים בכל העולם לפצח את חידת החורים השחורים אפופי המיסתורין, שעד לא מזמן היו בגדר... חור שחור. קוואזרים הם חורים שחורים על-מסיביים פעילים, כלומר חורים שחורים ענקיים הסופחים גז מסביבתם בקצב מסחרר. לקוואזרים בפרט, ולחורים שחורים על-מסיביים בכלל, תפקיד מרכזי בהיסטוריה של היקום. קצב גידולם קשור באופן הדוק להתפתחותן של מרבית הגלקסיות, והוא משפיע על צורתן ועל גודלן. עד כה לא ניתן היה למפות בדרך ישירה את מקומם ואת מהירותם של ענני הגז הסובבים חורים שחורים, למעט החור השחור שבמרכז הגלקסיה שלנו.
כעת, קבוצה בינלאומית של אסטרונומים, הכוללת אסטרונומים מאוניברסיטת תל אביב, השתמשה במכשיר חדש, GRAVITY, על מנת לצפות בלב ליבו של הקוואזר 3C273, ולראות, ישירות, את הגז הסובב את החור השחור. תוצאות התצפית המהפכנית התפרסמו בכתב העת היוקרתי Nature.
"לפני יותר מ-50 שנה זיהה האסטרונום מרטן שמידט עצם בהיר ביותר אך רחוק מאוד מאתנו, הקוואזר הראשון 3C273", מספר פרופ' חגי נצר מבית הספר לפיזיקה ולאסטרונומיה באוניברסיטת תל אביב, שהיה שותף לתצפית החדשה. "האנרגיה הנפלטת מעצם זה עולה עשרות מונים על האנרגיה הנפלטת מגלקסיית שביל החלב כולה, על כל 100 מיליארד הכוכבים שבה. למעשה, האנרגיה כה גדולה, עד שהדרך היחידה לייצרה היא על ידי הפיכת אנרגיית כבידה לחום, כלומר על ידי זרימה של כמויות גדולות של גז לתוככי חור שחור ענק".
כדי לצפות בדיסקת הגז הסובבת את הקוואזר 3C273, קבוצת המחקר הבינלאומית, בראשות אקהרד שטורם (Eckhard Sturm) וג'ייסון דקסטר (Jayson Dexter) ממכון מקס פלנק בגרמניה, השתמשה במכשיר חדש הנקרא GRAVITY. מדידות כאלה לא היו אפשריות עד עתה בגלל גודלו הזעיר של האזור בו נע החומר, בערך כגודלה של מערכת השמש, ומרחקו האדיר מאתנו – 2.5 מיליארד שנות אור. אולם GRAVITY מאפשר לחבר ארבעה טלסקופים ענקיים, כל אחד בקוטר של 8 מטרים, הנמצאים במצפה האירופאי הדרומי בצ'ילה, לכדי מערך הקרוי אינטרפרומטר שהוא בעל יכולת הפרדה השקולה לזו של טלסקופ יחיד בקוטר של 130 מטרים.
ההפרדה הזוויתית שמתקבלת מהמכשיר היא של 10 מיקרו-שניות קשת (החלק ה-100,000 של שניית קשת שהיא 1/3600 ממעלה של קשת). "יכולת הפרדה כזאת שקולה ליכולת למדוד מכדור הארץ את קטרו של מטבע של שני שקלים המונח על הירח", אומר פרופ' נצר.
יצוין כי מדידות מסוג שונה לחלוטין של אותם ענני גז, המתבססות על שינויים מהירים בעוצמת האור של קוואזרים, מתבצעות זה שנים. לדברי פרופ' חגי נצר, המדידות הראשונות של 3C273 בשיטה הקודמת נערכו במצפה הכוכבים ע"ש וייז באוניברסיטת תל אביב, ופורסמו בשנת 2000 בעבודת הדוקטור של שי כספי (כיום חוקר באוניברסיטת תל אביב), שעבד בהנחייתו של פרופ' נצר.
"השיטה החדשה, והמדויקת יותר, מאפשרת לקבוע תכונות רבות, כגון גודלו המדויק של האזור, כיוון התנועה של ענני הגז סביבו ואת מסתו המדויקת של החור השחור במרכז", אומר פרופ' נצר. "בעצם אנחנו מסתמכים כאן על חוקי קפלר. כפי שמודדים את מסת השמש לפי מהירות סיבוב כדור הארץ סביב השמש ומרחקו ממנה, כך מדדנו את מסת החור השחור לפי תנועת ענני הגז סביבו, והגענו ל-300 מיליון מסות שמש – תוצאה שהיא בהתאמה טובה לתוצאות שהתקבלו במצפה וייז".
ריינהרד גנזל (Reinhard Genzel) ממכון מקס פלנק, העומד בראש קבוצת המחקר אשר בנתה את המכשיר החדש, מציין את היכולת ליישם בעזרת GRAVITY שיטות שפותחו לחקר החור השחור במרכז גלקסיית שביל החלב לחורים שחורים בגלקסיות נוספות. "קבוצת המחקר עובדת היום על חמישה או שישה גופים אחרים בעלי תכונות דומות", מגלה פרופ' נצר. "בהמשך נבקש לקבל עוד זמן תצפית, ואני מאמין שאחרי מספר שנים נוכל להכליל את התוצאה גם לחורים שחורים קטנים יותר, גדולים יותר ורחוקים יותר, כלומר עתיקים יותר".
מחקר
התגלית מהווה עדות חדשה ומוחשית לתהליך מרתק של פירוק של גלקסיות ננסיות בידי גלקסיות גדולות יותר

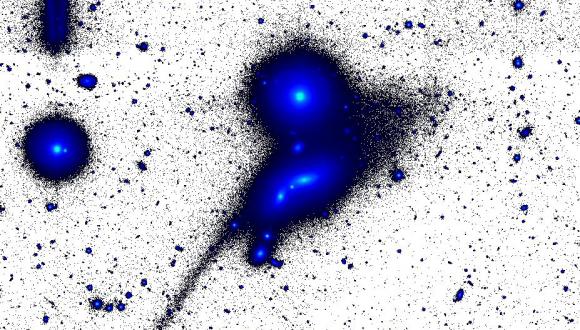
חוקרים מאוניברסיטת תל אביב, בהובלת ד"ר נח ברוש מבית הספר לפיסיקה ולאסטרונומיה, זיהו גוף שמימי בלתי מוכר במרחק של כ-300 מיליון שנות אור מאיתנו: מעין 'ראשן' עם 'ראש' אליפטי שבמרכזו שתי גלקסיות, ומאחוריו 'זנב' ענק באורך של כ-500,000 שנות אור. החוקרים סבורים כי התגלית מהווה עדות חדשה ומוחשית לתהליך מרתק ביקום: בליעתה של גלקסיה גמדית על ידי שתי הגלקסיות הגדולות שבקרבתה.
"אנחנו סבורים שזוהי עדות מוחשית לתהליך שמתרחש ביקום ללא הרף: פירוק של גלקסיות ננסיות בידי גלקסיות גדולות יותר," מסביר ד"ר נח ברוש מבית הספר לפיזיקה ולאסטרונומיה ע"ש ריימונד ובברלי סאקלר. "אירוע כזה, שאורך כמיליארד שנים, מתרחש כשהכוכבים של הגלקסיה הננסית נמשכים על ידי כוח הכבידה של הגלקסיות הגדולות".
"במקרה שלפנינו, ראש הראשן נוצר ככל הנראה מכוכבי הגלקסיה הננסית שהיו קרובים לשתי הגלקסיות 'הטורפות' הנצפות במרכז הראש, ואילו הזנב הענק מורכב משרידיהם של כוכבים רחוקים יותר בגלקסיה המתפרקת. למעשה התצפית שלנו לכדה את תהליך הפירוק בעיצומו".
"אנחנו מחפשים אקשן בשמיים. אנחנו צופים באופן תמידי בגלקסיות ובאזורים הקרובים אליהן כדי לזהות עדויות לשינויים. האם הגלקסיה גדלה או מצטמצמת? האם היא נמצאת באינטראקציה כלשהי עם גלקסיות נוספות?", ומוסיף "בתצפיות שלנו אנחנו עוקבים כבר זמן מה אחר קבוצות צפופות של גלקסיות, המכונות Hickson Compact Group HCG)), על שם האסטרונום הקנדי פול היקסון, שזיהה אותן ב-1982. ההנחה שככל שהן קרובות זו לזו יתרחשו ביניהן יותר פעילויות".
קבוצת הגלקסיות שנצפתה במחקר הנוכחי נקראת HCG 98. היא מורכבת מקבוצה צפופה של ארבע גלקסיות, ושוכנת במרחק 300 מיליון שנות אור מכדור הארץ. לשם השוואה, קצה היקום הנראה כיום נמצא במרחק כ-14 מיליארד שנות אור מכאן, כך שקבוצת HCG 98 היא למעשה 'שכנה' קרובה יחסית. התצפיות על קבוצת HCG 98 חשפו את הממצא החדש ויוצא הדופן, שלא התגלה עד היום מכיוון שהוא מאיר באור חיוור ביותר.
בתצפיות ובפיענוחן נעזרו האסטרונומים בטכנולוגיה מיוחדת: טלסקופ המאפשר תצפית וצילום של שטח נרחב יחסית בשמים, ובעל שיטת עיבוד המצרפת יחדיו תצלומים רבים של אותו אזור, המאפשרת לחוקרים להבחין גם בגופים חיוורים מאוד, שלא ניתן לראותם בדרך אחרת.
המחקר, בהובלת ד"ר ברוש, נערך בשיתוף עם מדענים באוניברסיטת קליפורניה בלוס אנג'לס ובאקדמיה הרוסית למדעים, והתצפיות בוצעו במצפה הכוכבים וייז שבמצפה רמון השייך לאוניברסיטת תל אביב, ועם טלסקופ זהה בארה"ב. מאמר אודותיו התפרסם בכתב העת המדעי של האגודה המלכותית לאסטרונומיה של בריטניה Monthly Notices of the Royal Astronomical Society.
בימים אלה ממשיכים החוקרים במצפה הכוכבים וייז בפרויקט גדול, שנעזר בטכנולוגיה המיוחדת לאיתור התרחשויות בסמוך לכמאה גלקסיות נוספות ברחבי היקום.

מחקר
חוקרים מאוניברסיטת תל אביב פיתחו טכנולוגיה להנדסת רקמות גוף להשתלה מפיסת שומן זעירה של המושתל עצמו

כיום, טכנולוגיית הנדסת הרקמות עושה שימוש בחומרים סינתטיים או כאלה שמקורם מבעלי חיים כדי להנדס או "לגדל" רקמות אנושיות לצרכים רפואיים. להליך זה יכולות להיות סכנות עבור המושתלים - לעתים הדבר מעורר תגובה חיסונית אצל המושתל, שמובילה לנטילת תרופות המדכאות את מערכת החיסון. פריצת דרך חדשה ממעבדות המחקר של אוניברסיטת תל אביב תאפשר לראשונה לייצר כל רקמה בגוף תוך התאמה אישית למושתל, מתוך פיסת שומן זעירה של המושתל עצמו, ומבלי להסתכן בדחיית השתל על ידי המערכת החיסונית. תוצאות המחקר פורץ הדרך התפרסמו בסוף השבוע בכתב העת היוקרתי Advanced Materials.
"רקמות גופנו מורכבות מתאים ומחומר חוץ-תאי, המקשר ביניהם מבחינה ביוכימית, מכנית וחשמלית", מסביר פרופ' טל דביר מהפקולטה למדעי החיים ע"ש ג'ורג' ס. וייז באוניברסיטת תל אביב, שהוביל את המחקר. "נכון להיום, לשם הנדסת רקמות משתמשים בחומר חוץ-תאי ממקור סינטתי או ביולוגי. החומר שנחשב לטוב ביותר לצורך השתלות נלקח מרקמות חזיר. בתהליך ההינדוס מוציאים את כל תאי החזיר, ובביו-חומר שנותר מגדלים תאים של בני אדם, אלא שאנו הראינו שחומר זה גורם לתגובה חיסונית חריפה, אשר עלולה לגרום לדחיית השתל".
כדי למצוא פתרון לבעיה, פרופ' דביר וצוותו השתמשו ברקמות שומניות של בני אדם. "תחילה הסרנו בניתוח זעיר פולשני רקמה שומנית מהחולה, הפרדנו את תאי השומן מהחומר החוץ-תאי וייצרנו ממנו ג'ל מותאם אישית לאדם זה", אומר פרופ' דביר. "בשלב השני 'תוכנתו מחדש' תאי השומן לתאי גזע פלוריפוטנטים, שיכולים להתמיין לכל תא בגוף שנבחר. כך הצלחנו לייצר רקמה לתיקון פציעות בחוט שדרה, לטיפול בשריר לב פגום, רקמה עצבית לחולי פרקינסון ורקמת שומן לניתוחי שחזור. כיוון שמקור הרקמות הוא מהחולה עצמו, הן לא יעוררו תגובה חיסונית", מדגיש פרופ' דביר. הטכנולוגיה כבר נבדקה בהצלחה על בעלי חיים ועל תאי מערכת החיסון של בני אדם.
פרופ' דביר מדגיש את המחיר הכבד שמשלמים היום חולים שעוברים השתלת רקמות שמקורן בבעלי חיים. "גם אם ההשתלה עוברת בהצלחה, המושתל עדיין צריך להמשיך ליטול, לפעמים למשך כל חייו, תרופות המדכאות את המערכת החיסונית, וכך הוא נותר חשוף ופגיע למחלות אחרות. רפואה מותאמת אישית היא העתיד. אמנם תהליך ההשתלה יהיה יקר יותר, לפחות בשנים הראשונות, אבל ברור שעדיף לבצע השתלה אחת מוצלחת, ללא כל חשש מתגובה חיסונית".
לאור ההצלחה הראשונית בודקים כעת פרופ' דביר וצוותו אפשרויות שונות להנדסת רקמות ועזרים רפואיים נוספים משומן חולים. בין החוקרים שפיתחו את הטכנולוגיה: ד"ר ראובן אדרי והדוקטורנטים עידן גל ונדב נור, בסיוע פרופ' דן פאר ופרופ' עירית גת ויקס מהמחלקה לחקר התא ואימונולוגיה, פרופ' דורון שבת מבית הספר לכימיה ופרופ' ליאור הלר מהמרכז הרפואי אסף הרופא.
"אנחנו כבר יודעים להנדס כמעט כל רקמה אפשרית, אבל לפנינו עוד דרך ארוכה", מסכם פרופ' דביר. "כבר הראינו שיפור לאחר השתלת הרקמה בחיות שעברו התקף לב ובחיות עם נזק לחוט השדרה, ובימים אלה אנחנו עובדים על הוכחת היכולת של שתלים עצביים המפרישים דופמין לטיפול במחלת הפרקינסון. עד היום הסברה הייתה שרקמות מחומר חוץ-תאי של חזירים בטוחות לשימוש, ולכן השימוש בהן היה נרחב במיוחד. כעת נוכל לייצר את כל העזרים הרפואיים כמו רשתות לבקע בטני ואפילו שסתומים ללב מהחולה עצמו, ובכך להימנע מסיבוכים הנובעים מדחיית השתל".